Kit de diagnóstico de antígeno de Helicobacter pylori (ensayo inmunocromatográfico de fluorescencia)
Kit de diagnóstico de antígeno para Helicobacter Pylori(Ensayo inmunocromatográfico de fluorescencia)
Sólo para uso diagnóstico in vitro
Lea atentamente este prospecto antes de usar y siga estrictamente las instrucciones. No se puede garantizar la fiabilidad de los resultados del ensayo si se observan desviaciones de las instrucciones de este prospecto.
USO PREVISTO
El kit de diagnóstico de antígeno de Helicobacter pylori (ensayo inmunocromatográfico de fluorescencia) es adecuado para la detección cuantitativa del antígeno HP en heces humanas mediante ensayo inmunocromatográfico de fluorescencia, lo cual tiene un importante valor diagnóstico complementario para infecciones gástricas. Toda muestra positiva debe confirmarse mediante otras metodologías. Esta prueba es para uso exclusivo de profesionales sanitarios.
RESUMEN
La infección gástrica por Helicobacter pylori está estrechamente relacionada con la gastritis crónica, la úlcera gástrica, el adenocarcinoma gástrico y el linfoma asociado a la mucosa gástrica. La tasa de infección por H. pylori es de aproximadamente el 90 % en pacientes con gastritis, úlcera gástrica, úlcera duodenal y cáncer gástrico. La Organización Mundial de la Salud ha identificado al H. pylori como el principal factor cancerígeno y constituye un claro factor de riesgo para el cáncer gástrico. La detección del H. pylori es de gran utilidad en el diagnóstico de la infección por H. pylori. La prueba, basada en técnicas de análisis inmunocromatográfico de fluorescencia, puede proporcionar resultados en 15 minutos.
PRINCIPIO DEL PROCEDIMIENTO
La tira cuenta con un anticuerpo anti-HP en la región de prueba, previamente fijado a la cromatografía de membrana. La almohadilla de la etiqueta está recubierta previamente con un anticuerpo anti-HP marcado con fluorescencia. Al analizar una muestra positiva, el HP presente en la muestra puede mezclarse con el anticuerpo anti-HP marcado con fluorescencia para formar una mezcla inmunitaria. Al permitir que la mezcla se mueva a lo largo de la tira de prueba, el complejo conjugado de HP es capturado por el anticuerpo anti-HP en la membrana y forma un complejo. La intensidad de la fluorescencia se correlaciona positivamente con el contenido de HP. El HP presente en la muestra puede detectarse mediante un analizador de inmunoensayo de fluorescencia.
REACTIVOS Y MATERIALES SUMINISTRADOS
Componentes del paquete 25T:
Tarjeta de prueba envuelta individualmente en una bolsa de aluminio con un desecante 25T
Diluyentes de muestra 25T
Prospecto 1
MATERIALES REQUERIDOS PERO NO PROPORCIONADOS
Recipiente para recogida de muestras, temporizador
RECOGIDA Y ALMACENAMIENTO DE MUESTRAS
1. Utilice un recipiente limpio y desechable para recolectar muestras de heces frescas y analícelas inmediatamente. Si no es posible realizar la prueba inmediatamente, consérvelas a 2-8 °C durante 3 días o a menos de -15 °C durante 6 meses.
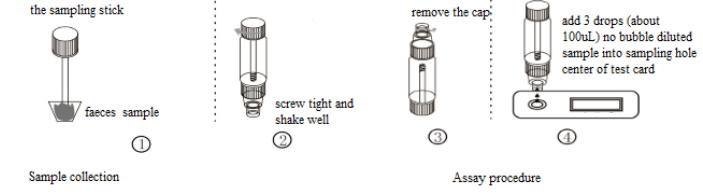
2. Saque la varilla de muestreo, introdúzcala en la muestra de heces, repita la acción 3 veces, tome las diferentes partes de la muestra de heces cada vez, luego vuelva a colocar la varilla de muestreo, atorníllela firmemente y agite bien, o use la varilla de muestreo para tomar aproximadamente 50 mg de muestra de heces y colóquela en un tubo de muestra de heces que contenga la dilución de la muestra y atorníllela firmemente.
3. Utilice una pipeta desechable para tomar la muestra de heces del paciente con diarrea, luego agregue 3 gotas (aproximadamente 100 µL) al tubo de muestreo fecal y agite bien.
Notas:
1. Evite los ciclos de congelación y descongelación.
2. Descongele las muestras a temperatura ambiente antes de usarlas.
PROCEDIMIENTO DE ENSAYO
Lea el manual de funcionamiento del instrumento y el prospecto antes de realizar la prueba.
1. Deje todos los reactivos y muestras a temperatura ambiente.
2. Abra el analizador inmunológico portátil (WIZ-A101), ingrese la contraseña de inicio de sesión de la cuenta de acuerdo con el método de operación del instrumento e ingrese a la interfaz de detección.
3. Escanee el código de identificación para confirmar el elemento de prueba.
4. Saque la tarjeta de prueba de la bolsa de aluminio.
5. Inserte la tarjeta de prueba en la ranura para tarjetas, escanee el código QR y determine el elemento de prueba.
6. Retire la tapa del tubo de muestra y deseche las primeras dos gotas de muestra diluida, agregue 3 gotas (aproximadamente 100 µL) de muestra diluida sin burbujas de manera vertical y lenta en el pocillo de muestra de la tarjeta con el dispensador provisto.
7. Haga clic en el botón "prueba estándar", después de 15 minutos, el instrumento detectará automáticamente la tarjeta de prueba, podrá leer los resultados desde la pantalla del instrumento y registrar/imprimir los resultados de la prueba.
8. Consulte las instrucciones del analizador inmunológico portátil (WIZ-A101).
VALORES ESPERADOS
HP-Ag<10
Se recomienda que cada laboratorio establezca su propio rango normal que represente su población de pacientes.
RESULTADOS E INTERPRETACIÓN DE LAS PRUEBAS
1. El HP-Ag en la muestra es superior a 10, lo que debería descartar un cambio en el estado fisiológico. Los resultados son anormales y deben diagnosticarse con síntomas clínicos.
2. Los resultados de este método sólo son aplicables a los rangos de referencia establecidos en este método y no existe comparabilidad directa con otros métodos.
3. Otros factores también pueden causar errores en los resultados de detección, incluidas razones técnicas, errores operativos y otros factores de muestra.
ALMACENAMIENTO Y ESTABILIDAD
1. El kit tiene una vida útil de 18 meses a partir de la fecha de fabricación. Conserve los kits no utilizados a una temperatura de 2-30 °C. NO CONGELAR. No utilizar después de la fecha de caducidad.
2. No abra la bolsa sellada hasta que esté listo para realizar una prueba, y se sugiere utilizar la prueba de un solo uso en el entorno requerido (temperatura 2-35 ℃, humedad 40-90 %) dentro de los 60 minutos lo más rápido posible.
3. El diluyente de muestra se utiliza inmediatamente después de abrirlo.
ADVERTENCIAS Y PRECAUCIONES
El kit debe estar sellado y protegido contra la humedad.
.Todas las muestras positivas deberán ser validadas mediante otras metodologías.
Todas las muestras deberán ser tratadas como contaminantes potenciales.
.NO utilice reactivo vencido.
.NO intercambie reactivos entre kits con diferentes números de lote.
NO reutilice las tarjetas de prueba ni ningún accesorio desechable.
.Un mal funcionamiento o una muestra excesiva o pequeña pueden provocar desviaciones en los resultados.
LIMITACIÓN
Al igual que con cualquier ensayo que emplee anticuerpos murinos, existe la posibilidad de interferencia de anticuerpos humanos antirratón (HAMA) en la muestra. Las muestras de pacientes que han recibido preparaciones de anticuerpos monoclonales para diagnóstico o tratamiento pueden contener HAMA. Dichas muestras pueden causar resultados falsos positivos o falsos negativos.
Este resultado de prueba es solo para referencia clínica, no debe servir como la única base para el diagnóstico y tratamiento clínico, el manejo clínico del paciente debe ser una consideración integral combinada con sus síntomas, historial médico, otros exámenes de laboratorio, respuesta al tratamiento, epidemiología y otra información.
Este reactivo se utiliza únicamente para análisis fecales. Es posible que no se obtengan resultados precisos al utilizarlo con otras muestras, como saliva, orina, etc.
CARACTERÍSTICAS DE RENDIMIENTO
| Linealidad | 10-1000 | desviación relativa: -15% a +15%. |
| Coeficiente de correlación lineal: (r) ≥ 0,9900 | ||
| Exactitud | La tasa de recuperación deberá estar entre el 85% – 115%. | |
| Repetibilidad | CV≤15% | |
RREFERENCIAS
1. Shao, JL y F. Wu. Avances recientes en los métodos de detección de Helicobacter pylori [J]. Revista de Gastroenterología y Hepatología, 2012, 21(8): 691-694
2.Hansen JH, et al. Interferencia de HAMA con inmunoensayos basados en anticuerpos monoclonales murinos[J].J of Clin Immunoassay, 1993, 16:294-299.
3. Levinson SS. La naturaleza de los anticuerpos heterofílicos y el papel en la interferencia del inmunoensayo [J]. J of Clin Immunoassay, 1992, 15:108-114.
Clave de símbolos utilizados:
 | Dispositivo médico de diagnóstico in vitro |
 | Fabricante |
 | Conservar entre 2 y 30 ℃ |
 | Fecha de expiración |
 | No reutilizar |
 | PRECAUCIÓN |
 | Consulte las instrucciones de uso |
Xiamen Wiz Biotech CO., LTD.
Dirección: Planta 3-4, Edificio n.º 16, Taller Biomédico, Carretera Oeste Wengjiao 2030, Distrito de Haicang, 361026, Xiamen, China
Teléfono: +86-592-6808278
Fax:+86-592-6808279