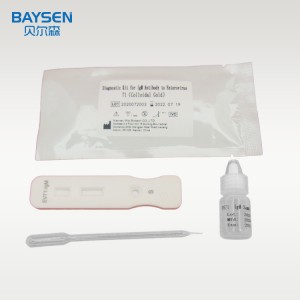
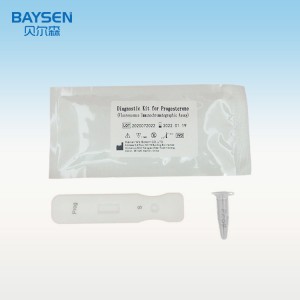
Kit de prueba rápida de anticuerpos IgM para Enterovirus 71 EV71 Anticuerpo EV 71
Parámetros del producto


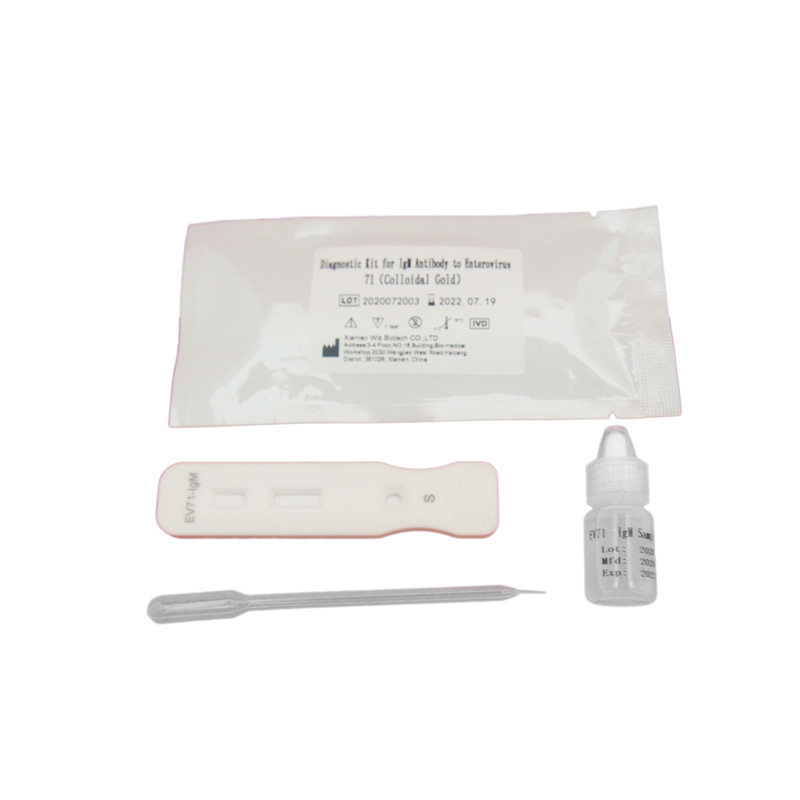
PRINCIPIO Y PROCEDIMIENTO DE LA PRUEBA FOB
PRINCIPIO
La membrana del dispositivo de prueba está recubierta con anticuerpo anti-EV71 en la región de prueba y anticuerpo de cabra anti-IgG de conejo en la región de control. La almohadilla de la etiqueta está recubierta previamente con anticuerpo anti-EV71 marcado con fluorescencia e IgG de conejo. Al analizar una muestra positiva, el antígeno EV71 presente en la muestra se combina con el anticuerpo anti-EV71 marcado con fluorescencia y forma una mezcla inmunitaria. Bajo la acción de la cromatografía, el complejo fluye hacia el papel absorbente y, al atravesar la región de prueba, se combina con el anticuerpo anti-EV71, formando un nuevo complejo.
Si es negativo, la muestra no contiene anticuerpos IgM contra el enterovirus 71, por lo que no se puede formar el complejo inmune. No habrá una línea roja en el área de detección (T). Independientemente de si el anticuerpo IgM contra el enterovirus 71 está presente en la muestra o no, el anticuerpo monoclonal anti-IgM humana de ratón marcado con oro coloidal restante y el anticuerpo IgG anti-ratón de cabra recubierto en el área de control de calidad (C) se unen. Luego, los aglutinados desarrollan color en el área de control de calidad, y aparecerá la línea roja en (C). La línea roja es el estándar que aparece en el área de control de calidad (C) para juzgar si hay suficientes muestras y si el proceso cromatográfico es normal. También se utiliza como estándar de control interno para reactivos.
Procedimiento de prueba:
1. Las muestras analizadas pueden ser de sangre completa, incluyendo sangre venosa o periférica. La sangre completa no se puede almacenar después de su recolección. Debe utilizarse inmediatamente después de su recolección.
2. Las muestras de suero se recolectan asépticamente según las técnicas estándar. No se puede usar suero inactivado por calor. No se recomienda usar suero lipémico, turbio o contaminado. La presencia de partículas en el suero y la precipitación afectarán los resultados de la prueba; estas muestras deben centrifugarse o filtrarse antes de su uso.
3.Las muestras analizadas pueden ser plasma con heparina, citrato de sodio o anticoagulante EDTA.
4. Según las técnicas estándar, tome la muestra. La muestra de suero o plasma puede conservarse refrigerada a 2-8 °C durante 3 días y criopreservada a -15 °C durante 3 meses.
5.Todas las muestras evitan los ciclos de congelación y descongelación.

Sobre nosotros

Xiamen Baysen Medical Tech Limited es una empresa de alta tecnología biológica dedicada al campo de los reactivos de diagnóstico rápido, que integra la investigación, el desarrollo, la producción y las ventas en un todo. La empresa cuenta con un equipo de investigación avanzado y gerentes de ventas, todos con amplia experiencia laboral en empresas biofarmacéuticas chinas e internacionales.
Visualización del certificado