Kit de diagnóstico de insulina para el manejo de la diabetes
Kit de diagnóstico para insulina
Metodología: Ensayo inmunocromatográfico de fluorescencia
Información de producción
| Número de modelo | INS | Embalaje | 25 pruebas/kit, 30 kits/caja |
| Nombre | Kit de diagnóstico para insulina | Clasificación de instrumentos | Clase II |
| Características | Alta sensibilidad, fácil operación. | Certificado | CE/ISO13485 |
| Exactitud | > 99% | Duración | Dos años |
| Metodología | Ensayo inmunocromatográfico de fluorescencia | Servicio OEM/ODM | Disponible |
Superioridad
Tiempo de prueba: 10-15 minutos
Almacenamiento: 2-30 °C/36-86 °F
Metodología: Ensayo inmunocromatográfico de fluorescencia

USO PREVISTO
Este kit es adecuado para la determinación cuantitativa in vitro de los niveles de insulina (INS) en muestras de suero, plasma o sangre completa humanas para evaluar la función de las células β de los islotes pancreáticos. Este kit solo proporciona resultados de la prueba de insulina (INS), y el resultado obtenido debe analizarse junto con otra información clínica.
Característica:
• Alta sensibilidad
• lectura del resultado en 15 minutos
• Fácil operación
• Alta precisión
Procedimiento de prueba
| 1 | Antes de utilizar el reactivo, lea atentamente el prospecto del paquete y familiarícese con los procedimientos de operación. |
| 2 | Seleccione el modo de prueba estándar del analizador inmunológico portátil WIZ-A101 |
| 3 | Abra el paquete de reactivo envuelto en papel de aluminio y saque el dispositivo de prueba. |
| 4 | Inserte horizontalmente el dispositivo de prueba en la ranura del analizador inmunológico. |
| 5 | En la página de inicio de la interfaz de operación del analizador inmunológico, haga clic en “Estándar” para ingresar a la interfaz de prueba. |
| 6 | Haga clic en “QC Scan” para escanear el código QR en el lado interior del kit; ingrese los parámetros relacionados con el kit en el instrumento y seleccione el tipo de muestra. Nota: Cada número de lote del kit se escaneará una sola vez. Si ya se ha escaneado el número de lote, omita este paso. |
| 7 | Verifique la coherencia del “Nombre del producto”, “Número de lote”, etc. en la interfaz de prueba con la información de la etiqueta del kit. |
| 8 | Saque el diluyente de muestra según la información consistente, agregue 10 μL de muestra de suero/plasma/sangre completa y mézclelos completamente; |
| 9 | Agregue 80 µL de la solución completamente mezclada antes mencionada en el pocillo del dispositivo de prueba; |
| 10 | Después de agregar completamente la muestra, haga clic en “Tiempo” y el tiempo de prueba restante se mostrará automáticamente en la interfaz. |
| 11 | El analizador inmunológico completará automáticamente la prueba y el análisis cuando se alcance el tiempo de prueba. |
| 12 | Una vez completada la prueba con el analizador inmunológico, el resultado de la prueba se mostrará en la interfaz de prueba o se podrá ver a través de “Historial” en la página de inicio de la interfaz de operación. |
Nota: cada muestra deberá pipetearse con una pipeta desechable limpia para evitar la contaminación cruzada.
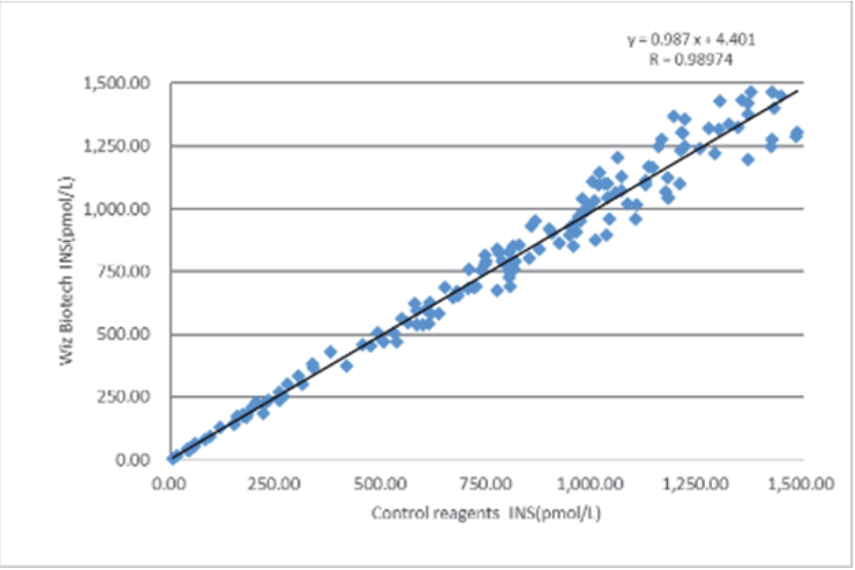
Rendimiento clínico
El rendimiento de la evaluación clínica de este producto se evaluó mediante la recolección de 173 muestras clínicas. Los resultados de las pruebas se compararon utilizando los kits correspondientes del método de electroquimioluminiscencia comercializado como reactivos de referencia. Su comparabilidad se investigó mediante regresión lineal. Los coeficientes de correlación de ambas pruebas fueron y = 0,987x + 4,401 y R = 0,9874, respectivamente.