Kit de diagnóstico para troponina I cardíaca, mioglobina e isoenzima MB da creatina quinase.
Kit de diagnóstico para troponina I cardíaca/isoenzima MB da creatina quinase/mioglobina
Metodologia: Ensaio imunocromatográfico de fluorescência
Informações sobre a produção
| Número do modelo | cTnI/CK-MB/MYO | Embalagem | 25 testes/kit, 30 kits/caixa |
| Nome | Kit de diagnóstico para troponina I cardíaca/isoenzima MB da creatina quinase/mioglobina | Classificação de instrumentos | Classe II |
| Características | Alta sensibilidade, fácil operação. | Certificado | CE/ ISO13485 |
| Precisão | > 99% | Prazo de validade | Dois anos |
| Metodologia | Ensaio de imunocromatografia de fluorescência | Serviço OEM/ODM | Disponível |
USO PRETENDIDO
Este kit é aplicável à detecção quantitativa in vitro de concentrações de marcadores de lesão miocárdica em pacientes cardíacos.
troponina I, isoenzima MB da creatina quinase e mioglobina em amostras de soro/plasma/sangue total humano, e
É indicado para o diagnóstico auxiliar de infarto do miocárdio. Este kit fornece apenas os resultados do teste de troponina I cardíaca.
isoenzima MB da creatina quinase e mioglobina, e os resultados obtidos devem ser usados em combinação com outros.
Informação clínica para análise. Deve ser utilizada apenas por profissionais de saúde.
Procedimento de teste
| 1 | Antes de usar o reagente, leia atentamente a bula e familiarize-se com os procedimentos de operação. |
| 2 | Selecione o modo de teste padrão do analisador imunológico portátil WIZ-A101. |
| 3 | Abra a embalagem de alumínio contendo o reagente e retire o dispositivo de teste. |
| 4 | Insira o dispositivo de teste horizontalmente na ranhura do analisador imunológico. |
| 5 | Na página inicial da interface de operação do analisador imunológico, clique em “Padrão” para acessar a interface de teste. |
| 6 | Clique em “Escanear QC” para escanear o código QR na parte interna do kit; insira os parâmetros relacionados ao kit no instrumento e selecione o tipo de amostra. Observação: Cada número de lote do kit deve ser escaneado apenas uma vez. Se o número do lote já tiver sido escaneado, ignore esta etapa. |
| 7 | Verifique a consistência do “Nome do Produto”, “Número do Lote”, etc., na interface de teste com as informações no rótulo do kit. |
| 8 | Após obter informações consistentes, retire o diluente da amostra, adicione 80 μL da amostra de soro/plasma/sangue total e misture bem; |
| 9 | Adicione 80 µL da solução previamente misturada no poço do dispositivo de teste; |
| 10 | Após adicionar todas as amostras, clique em “Cronometragem” e o tempo restante do teste será exibido automaticamente na interface. |
| 11 | O analisador imunológico concluirá automaticamente o teste e a análise quando o tempo de teste for atingido. |
| 12 | Após a conclusão do teste pelo analisador imunológico, o resultado será exibido na interface de teste ou poderá ser visualizado através do "Histórico" na página inicial da interface de operação. |
Nota: cada amostra deve ser pipetada com uma pipeta descartável limpa para evitar contaminação cruzada.
Superioridade
Tempo de teste: 10-15 minutos
Armazenamento: 2-30℃/36-86℉
Metodologia: Ensaio imunocromatográfico de fluorescência
Recurso:
• Alta sensibilidade
• Resultado em 15 minutos
• Operação fácil
• 3 testes de uma só vez, economizando tempo.
• Alta precisão
O desempenho clínico
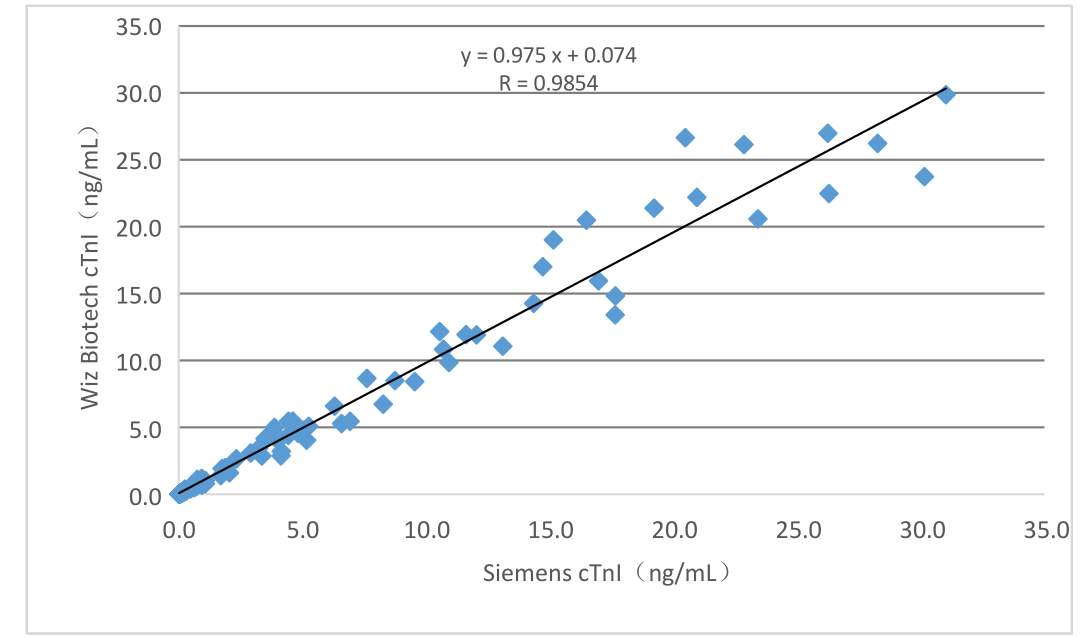
O desempenho clínico deste produto foi avaliado através da coleta de 150 amostras clínicas.
a) No caso do item cTnI, o kit comercial correspondente de ensaio de quimioluminescência utilizado como reagente de referência,
Os resultados da detecção foram comparados e sua comparabilidade foi estudada por meio de regressão linear.
Os coeficientes de correlação dos dois ensaios são Y=0,975X+0,074 e R=0,9854, respectivamente;
b) No caso do item CK-MB, o kit comercial correspondente de ensaios de eletroquimioluminescência foi utilizado como referência.
Os reagentes e os resultados da detecção foram comparados e sua comparabilidade foi estudada por meio de análise linear.
Os coeficientes de regressão e correlação dos dois ensaios são Y=0,915X+0,242 e R=0,9885, respectivamente.
c) No caso de um produto MYO, o kit comercial correspondente de imunoensaios de fluorescência com resolução temporal foi utilizado como referência.
Os reagentes e os resultados da detecção foram comparados e sua comparabilidade foi estudada por meio de análise linear.
Os coeficientes de regressão e correlação dos dois ensaios são y=0,989x+2,759 e R=0,9897, respectivamente.
Você também pode gostar de: