Anticorpi IgM Enterovirus 71 EV71 kit per test rapido EV 71 anticorpi
Parametri del prodotto


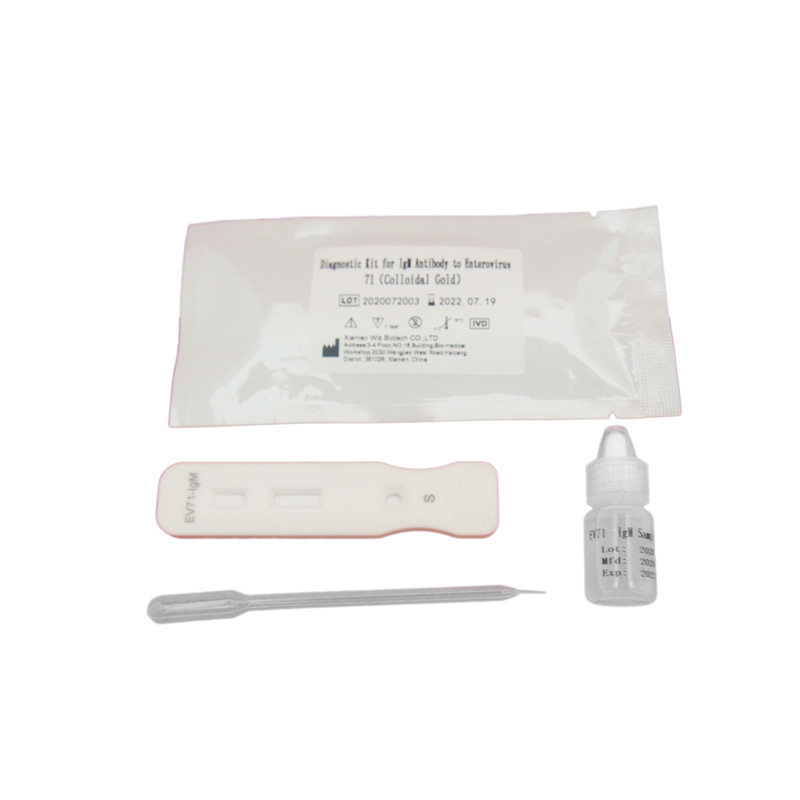
PRINCIPIO E PROCEDURA DEL TEST FOB
PRINCIPIO
La membrana del dispositivo di test è rivestita con anticorpo anti-EV71 nella regione di test e con anticorpo anti-IgG di coniglio di capra nella regione di controllo. I tamponi di etichettatura sono preventivamente rivestiti con anticorpo anti-EV71 marcato con fluorescenza e IgG di coniglio. Quando si analizza un campione positivo, l'antigene EV71 presente nel campione si lega all'anticorpo anti-EV71 marcato con fluorescenza, formando una miscela immunitaria. Sotto l'azione della cromatografia, il complesso fluisce nella direzione della carta assorbente e, quando attraversa la regione di test, si lega all'anticorpo anti-EV71 di rivestimento, formando un nuovo complesso.
Se il risultato è negativo, il campione non contiene anticorpi IgM contro l'enterovirus 71, quindi non si può formare l'immunocomplesso. Non ci sarà alcuna linea rossa nell'area di rilevamento (T). Indipendentemente dalla presenza o meno di anticorpi IgM contro l'enterovirus 71 nel campione, l'anticorpo monoclonale anti-IgM umano di topo marcato con oro colloidale e l'anticorpo anti-IgG di capra di topo, immobilizzati nell'area di controllo qualità (C), si legano. Successivamente, gli agglutinati sviluppano colore nell'area di controllo qualità e apparirà una linea rossa in (C). La linea rossa che appare nell'area di controllo qualità (C) è lo standard utilizzato per valutare se ci sono campioni a sufficienza e se il processo cromatografico è normale. Viene anche utilizzata come standard di controllo interno per i reagenti.
Procedura di prova:
1. I campioni analizzati possono essere sangue intero, compreso il sangue venoso o il sangue periferico. Il sangue intero non può essere conservato dopo il prelievo. Deve essere utilizzato subito dopo il prelievo.
2. I campioni di siero vengono raccolti in modo asettico secondo tecniche standard. Il siero inattivato termicamente non può essere utilizzato. Si sconsiglia l'uso di siero lipemico, torbido o contaminato. La presenza di particelle nel siero e di precipitati può influenzare i risultati del test; pertanto, tali campioni devono essere centrifugati o filtrati prima dell'uso.
3. I campioni analizzati possono essere plasma anticoagulante con eparina, citrato di sodio o EDTA.
4. Secondo le tecniche standard, raccogliere il campione. Il campione di siero o plasma può essere conservato in frigorifero a 2-8 °C per 3 giorni e crioconservato a temperature inferiori a -15 °C per 3 mesi.
5. Tutti i campioni devono essere sottoposti a cicli di congelamento e scongelamento.

Chi siamo

Xiamen Baysen Medical Tech Limited è un'azienda altamente specializzata nel settore dei reagenti per la diagnostica rapida, che integra ricerca e sviluppo, produzione e vendita. L'azienda si avvale di un team di ricercatori altamente qualificati e di responsabili commerciali con una solida esperienza maturata in aziende biofarmaceutiche cinesi e internazionali.
Esposizione del certificato