Gestione del diabete, insulina, kit diagnostico
Kit diagnostico per l'insulina
Metodologia: Saggio immunocromatografico a fluorescenza
Informazioni sulla produzione
| Numero di modello | INS | Imballaggio | 25 test/kit, 30 kit/cartone |
| Nome | Kit diagnostico per l'insulina | Ciclo degli strumenti | Classe II |
| Caratteristiche | Elevata sensibilità, facile utilizzo | Certificato | CE/ ISO13485 |
| Precisione | > 99% | durata di conservazione | Due anni |
| Metodologia | Saggio immunocromatografico a fluorescenza | Servizio OEM/ODM | Disponibile |
Superiorità
Tempo di prova: 10-15 minuti
Conservazione: 2-30℃/36-86℉
Metodologia: Saggio immunocromatografico a fluorescenza

USO PREVISTO
Questo kit è adatto per la determinazione quantitativa in vitro dei livelli di insulina (INS) in campioni di siero/plasma/sangue intero umano per la valutazione della funzione delle cellule β delle isole pancreatiche. Questo kit fornisce solo i risultati del test dell'insulina (INS) e il risultato ottenuto deve essere analizzato in combinazione con altre informazioni cliniche.
Caratteristica:
• Alta sensibilità
• Risultato disponibile in 15 minuti
• Funzionamento semplice
• Elevata precisione
Procedura di prova
| 1 | Prima di utilizzare il reagente, leggere attentamente il foglietto illustrativo e familiarizzarsi con le procedure operative. |
| 2 | Selezionare la modalità di test standard dell'analizzatore immunologico portatile WIZ-A101. |
| 3 | Aprire la bustina di alluminio contenente il reagente ed estrarre il dispositivo di test. |
| 4 | Inserire orizzontalmente il dispositivo di test nell'apposito alloggiamento dell'analizzatore immunologico. |
| 5 | Nella pagina iniziale dell'interfaccia operativa dell'analizzatore immunologico, fare clic su "Standard" per accedere all'interfaccia di test. |
| 6 | Fare clic su "QC Scan" per scansionare il codice QR sul lato interno del kit; inserire i parametri relativi al kit nello strumento e selezionare il tipo di campione. Nota: ogni numero di lotto del kit deve essere scansionato una sola volta. Se il numero di lotto è già stato scansionato, saltare questo passaggio. |
| 7 | Verificare la coerenza di "Nome prodotto", "Numero di lotto" ecc. nell'interfaccia di test con le informazioni riportate sull'etichetta del kit. |
| 8 | Prelevare il diluente del campione in base alle informazioni disponibili, aggiungere 10 μL di siero/plasma/campione di sangue intero e mescolare accuratamente; |
| 9 | Aggiungere 80 µL della suddetta soluzione accuratamente miscelata nel pozzetto del dispositivo di prova; |
| 10 | Una volta completato l'inserimento dei campioni, fare clic su "Tempi" e il tempo di prova rimanente verrà visualizzato automaticamente nell'interfaccia. |
| 11 | L'analizzatore immunitario completerà automaticamente il test e l'analisi allo scadere del tempo previsto. |
| 12 | Una volta completato il test con l'analizzatore immunologico, il risultato verrà visualizzato sull'interfaccia del test oppure potrà essere consultato tramite la sezione "Cronologia" nella pagina principale dell'interfaccia operativa. |
Nota: ogni campione deve essere pipettato utilizzando una pipetta monouso pulita per evitare la contaminazione incrociata.
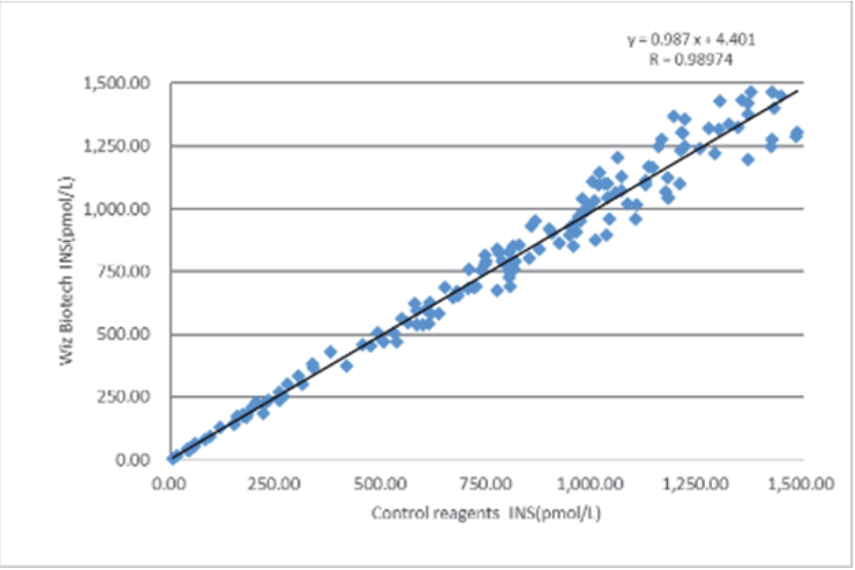
Prestazioni cliniche
Le prestazioni cliniche di questo prodotto sono state valutate raccogliendo 173 campioni clinici. I risultati dei test sono stati confrontati utilizzando i corrispondenti kit del metodo di elettrochemiluminescenza commercializzato come reagenti di riferimento, e la loro comparabilità è stata studiata mediante regressione lineare, e i coefficienti di correlazione dei due test sono risultati rispettivamente y = 0,987x + 4,401 e R = 0,9874.