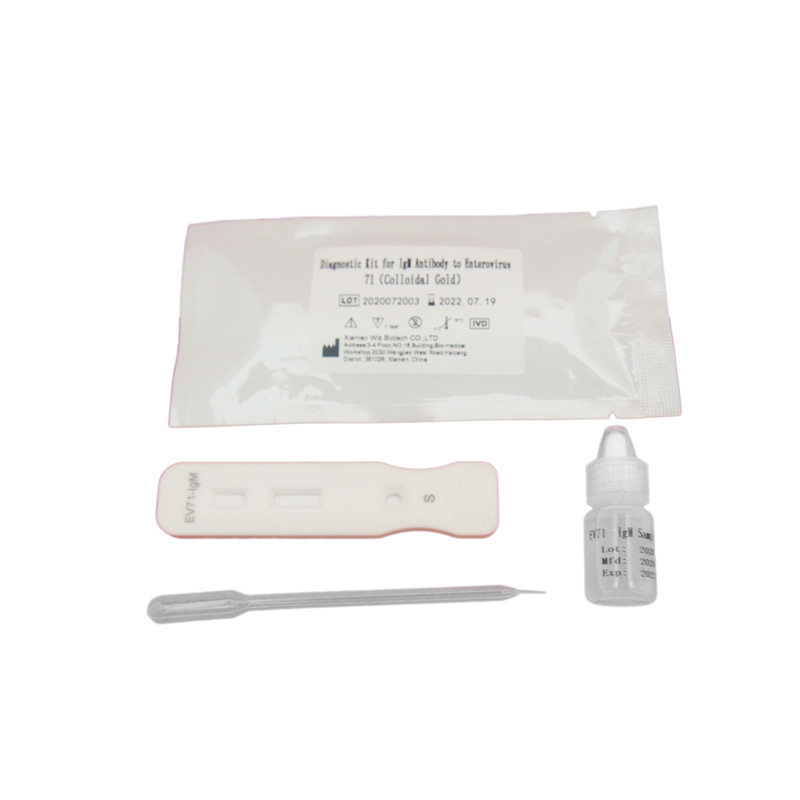
Kit de proba rápida de anticorpos IgM para enterovirus 71 EV71 anticorpos EV 71
Parámetros dos produtos


PRINCIPIO E PROCEDEMENTO DA PROBA FOB
PRINCIPIO
A membrana do dispositivo de proba está recuberta cun anticorpo anti-EV71 na rexión de proba e cun anticorpo IgG de cabra anti-coello na rexión de control. As etiquetas están recubertas previamente cun anticorpo anti-EV71 marcado con fluorescencia e IgG de coello. Ao obter unha mostra positiva, o antíxeno EV71 da mostra combínase co anticorpo anti-EV71 marcado con fluorescencia e forma unha mestura inmunitaria. Baixo a acción da cromatografía, o complexo flúe na dirección do papel absorbente; cando o complexo pasa pola rexión de proba, combínase co anticorpo de revestimento anti-EV71, formando un novo complexo.
Se é negativo, a mostra non contén anticorpos IgM contra o enterovirus 71, polo que non se pode formar o complexo inmunitario. Non haberá unha liña vermella na área de detección (T). Independentemente de que exista ou non anticorpo IgM contra o enterovirus 71 na mostra, únense o anticorpo monoclonal IgM antihumano de rato marcado con ouro coloidal restante e o anticorpo IgG de cabra antirato revestido na área de control de calidade (C). Despois, os aglutinados desenvolven cor na área de control de calidade e aparecerá a liña vermella en (C). A liña vermella é o estándar que aparece na área de control de calidade (C) para xulgar se hai mostras suficientes e se o proceso de cromatografía é normal. Tamén se usa como estándar de control interno para reactivos.
Procedemento de proba:
1. As mostras analizadas poden ser sangue enteiro, incluído sangue venoso ou sangue periférico. O sangue enteiro non se pode almacenar despois da recollida. Debe usarse pouco despois da recollida.
2. As mostras de soro recóllense de forma aséptica segundo as técnicas estándar. Non se pode usar soro inactivado pola calor. Non se recomenda o uso de soro lipémico, turbio ou contaminado. A presenza de materia particulada no soro e a precipitación afectarán os resultados da proba, polo que estas mostras deben centrifugarse ou filtrarse antes do seu uso.
3. As mostras analizadas poden ser heparina, citrato de sodio ou plasma anticoagulante con EDTA.
4. Recóllese a mostra segundo as técnicas estándar. A mostra de soro ou plasma pódese conservar refrixerada a 2-8 ℃ durante 3 días e crioconservarse por debaixo de -15 ℃ durante 3 meses.
5. Todas as mostras deben evitar os ciclos de conxelación e desconxelación.

Sobre nós

Xiamen Baysen Medical Tech Limited é unha empresa de alta bioloxía dedicada ao sector dos reactivos de diagnóstico rápido e que integra a investigación e o desenvolvemento, a produción e as vendas nun todo. A empresa conta con moitos investigadores avanzados e xerentes de vendas, todos eles con ampla experiencia laboral en empresas biofarmacéuticas chinesas e internacionais.
Visualización do certificado