Kit de diagnóstico para a troponina I cardíaca, mioglobina e isoenzima MB da creatina quinase
Kit de diagnóstico para a troponina I cardíaca ∕Isoenzima MB da creatina quinase ∕Mioglobina
Metodoloxía: Ensaio inmunocromatográfico de fluorescencia
Información de produción
| Número de modelo | cTnI/CK-MB/MYO | Embalaxe | 25 probas/kit, 30 kits/caixa |
| Nome | Kit de diagnóstico para a troponina I cardíaca ∕Isoenzima MB da creatina quinase ∕Mioglobina | Clasificación de instrumentos | Clase II |
| Características | Alta sensibilidade, fácil funcionamento | Certificado | CE/ISO13485 |
| Precisión | > 99% | Vida útil | Dous anos |
| Metodoloxía | Ensaio inmunocromatográfico de fluorescencia | Servizo OEM/ODM | Dispoñible |
USO PREVISTO
Este kit é aplicable á detección cuantitativa in vitro de concentracións de marcadores de lesión miocárdica de enfermidades cardíacas.
troponina I, isoenzima MB da creatina quinaseína e mioglobina en mostras de soro/plasma/sangue completo humano e
É axeitado para o diagnóstico auxiliar do infarto de miocardio. Este kit só proporciona resultados das probas da troponina I cardíaca,
isoenzima MB da creatina quinaseína e da mioglobina, e os resultados obtidos utilizaranse en combinación con outros
información clínica para a súa análise. Só debe ser empregada por profesionais sanitarios.
Procedemento de proba
| 1 | Antes de usar o reactivo, lea atentamente o prospecto e familiarícese cos procedementos operativos. |
| 2 | Seleccionar o modo de proba estándar do analizador inmunitario portátil WIZ-A101 |
| 3 | Abra o envase de reactivos na bolsa de aluminio e retire o dispositivo de proba. |
| 4 | Insira horizontalmente o dispositivo de proba na ranura do analizador inmunitario. |
| 5 | Na páxina de inicio da interface de funcionamento do analizador inmunitario, prema en "Estándar" para acceder á interface de proba. |
| 6 | Fai clic en "Escanear QC" para escanear o código QR que se atopa no interior do kit; introduce os parámetros relacionados co kit no instrumento e selecciona o tipo de mostra. Nota: Cada número de lote do kit debe ser escaneado unha vez. Se o número de lote xa foi escaneado, omita este paso. |
| 7 | Comprobe a coherencia de "Nome do produto", "Número de lote" etc. na interface de proba coa información da etiqueta do kit. |
| 8 | Retirar o diluínte da mostra cando se obteña información consistente, engadir 80 μL de mostra de soro/plasma/sangue completo e mesturar ben; |
| 9 | Engadir 80 µL da solución ben mesturada mencionada anteriormente ao pozo do dispositivo de proba; |
| 10 | Despois de completar a adición da mostra, prema en "Tempo" e o tempo restante da proba mostrarase automaticamente na interface. |
| 11 | O analizador inmunitario completará automaticamente a proba e a análise cando se chegue á hora da proba. |
| 12 | Unha vez finalizada a proba co analizador inmunitario, o resultado da proba mostrarase na interface de proba ou poderá verse a través do "Historial" na páxina de inicio da interface de operación. |
Nota: cada mostra debe pipetearse cunha pipeta desbotable limpa para evitar a contaminación cruzada.
Superioridade
Tempo de proba: 10-15 minutos
Almacenamento: 2-30 ℃/36-86 ℉
Metodoloxía: Ensaio inmunocromatográfico de fluorescencia
Característica:
• Alta sensibilidade
• lectura de resultados en 15 minutos
• Fácil de usar
• 3 probas á vez, aforrando tempo.
• Alta precisión
O rendemento clínico
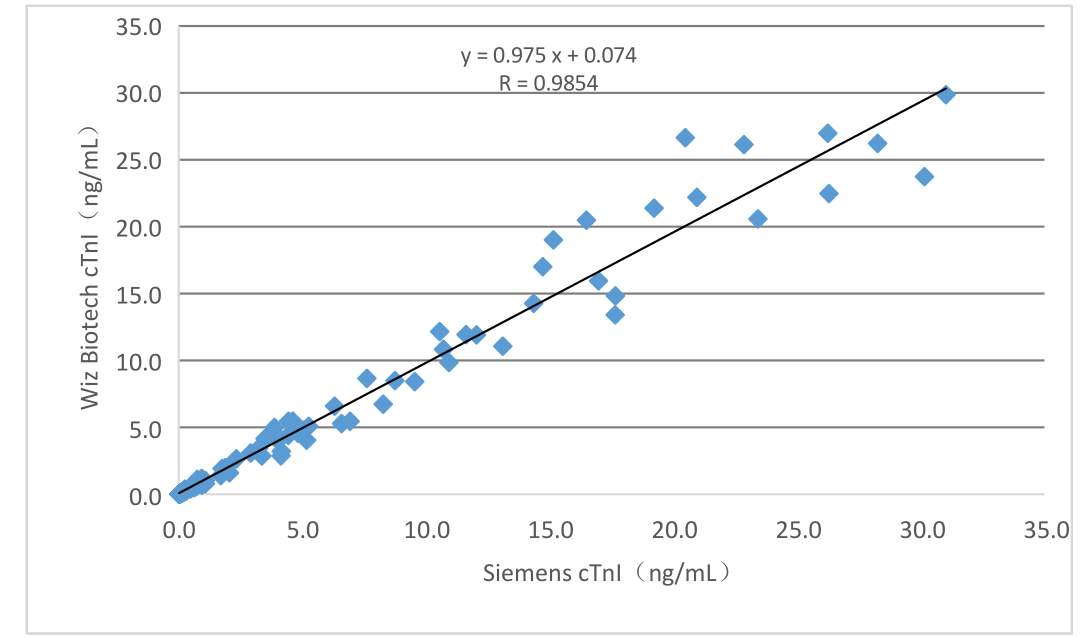
O rendemento clínico deste produto avaliouse mediante a recollida de 150 casos de mostras clínicas.
a) No caso do artigo cTnI, o kit comercializado correspondente de ensaios de quimioluminiscencia utilizado como reactivo de referencia,
comparáronse os resultados da detección e estudouse a súa comparabilidade mediante regresión lineal e
os coeficientes de correlación dos dous ensaios son Y = 0,975X + 0,074 e R = 0,9854 respectivamente;
b) No caso do artigo CK-MB, o kit comercializado correspondente de ensaios de electroquimioluminiscencia utilizado como referencia.
reactivo, comparáronse os resultados da detección e estudouse a súa comparabilidade mediante métodos lineais
regresión e os coeficientes de correlación dos dous ensaios son Y=0,915X+0,242 e R=0,9885 respectivamente.
c) No caso do artigo MYO, o kit comercializado correspondente de inmunoensaios de fluor con resolución temporal utilizado como referencia.
reactivo, comparáronse os resultados da detección e estudouse a súa comparabilidade mediante métodos lineais
regresión e os coeficientes de correlación dos dous ensaios son y=0,989x+2,759 e R=0,9897 respectivamente.
Tamén che pode gustar: