Kit de test rapide combiné Pepsinogène I, Pepsinogène II et Gastrine-17
Kit de diagnostic pour le pepsinogène I/pepsinogène II/gastrine-17
Méthodologie : dosage immunochromatographique par fluorescence
Informations sur la production
| Numéro de modèle | G17/PGI/PGII | Emballage | 25 tests/kit, 30 kits/carton |
| Nom | Kit de diagnostic pour le pepsinogène I/pepsinogène II/gastrine-17 | Classification des instruments | Classe II |
| Caractéristiques | Haute sensibilité, utilisation facile | Certificat | CE/ ISO 13485 |
| Précision | > 99% | durée de conservation | Deux ans |
| Méthodologie | dosage immunochromatographique par fluorescence | Service OEM/ODM | Disponible |
UTILISATION PRÉVUE
Ce kit est applicable à la détection quantitative in vitro de la concentration de pepsinogène I (PGI) et de pepsinogène II.
(PGII) et la gastrine 17 dans des échantillons de sérum/plasma/sang total humains, afin d'évaluer les cellules des glandes oxyntiques gastriques
Fonction, lésion de la muqueuse du fundus gastrique et gastrite atrophique. Le kit fournit uniquement le résultat du test du pepsinogène I
(PGI), Pepsinogène II (PGII) et Gastrine 17. Le résultat obtenu sera analysé en combinaison avec d'autres données cliniques.
Ces informations ne doivent être utilisées que par les professionnels de la santé.
Procédure de test
| 1 | Avant d'utiliser le réactif, veuillez lire attentivement la notice d'emballage et vous familiariser avec le mode d'emploi. |
| 2 | Sélectionnez le mode de test standard de l'analyseur immunitaire portable WIZ-A101. |
| 3 | Ouvrez le sachet en aluminium contenant le réactif et sortez le dispositif de test. |
| 4 | Insérer horizontalement le dispositif de test dans la fente de l'analyseur immunitaire. |
| 5 | Sur la page d'accueil de l'interface de fonctionnement de l'analyseur immunitaire, cliquez sur « Standard » pour accéder à l'interface de test. |
| 6 | Cliquez sur « QC Scan » pour scanner le code QR situé à l’intérieur du kit ; saisissez les paramètres relatifs au kit dans l’instrument et Sélectionnez le type d'échantillon. Remarque : Chaque numéro de lot du kit doit être scanné une seule fois. Si le numéro de lot a été scanné, alors Passez cette étape. |
| 7 | Vérifiez la cohérence des informations « Nom du produit », « Numéro de lot », etc., sur l’interface de test, en vous référant au kit. étiquette. |
| 8 | Une fois la cohérence des informations confirmée, retirez le diluant de l'échantillon et ajoutez 80 µL de sérum/plasma/sang total. échantillonner et mélanger suffisamment. |
| 9 | Ajouter 80 µL de la solution mélangée ci-dessus dans l'orifice d'échantillon du dispositif de test. |
| 10 | Une fois l'échantillon entièrement ajouté, cliquez sur « Chronométrage » et le temps de test restant s'affichera automatiquement. interface. |
| 11 | L'analyseur immunitaire effectuera automatiquement le test et l'analyse lorsque le temps imparti sera écoulé. |
| 12 | Calcul et affichage des résultats Une fois le test effectué par l'analyseur immunitaire terminé, le résultat s'affichera sur l'interface de test ou pourra être consulté. via « Historique » sur la page d’accueil de l’interface utilisateur. |
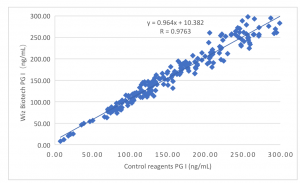
La performance clinique
L'efficacité clinique du produit est évaluée par la collecte de 200 échantillons cliniques. Le kit ELISA commercialisé est utilisé comme réactif de contrôle. Les résultats du test PGI sont comparés. Une régression linéaire est utilisée pour étudier leur comparabilité. Les coefficients de corrélation des deux tests sont respectivement y = 0,964X + 10,382 et R = 0,9763. Les résultats du test PGII sont comparés. Une régression linéaire est utilisée pour étudier leur comparabilité. Les coefficients de corrélation des deux tests sont respectivement y = 1,002X + 0,025 et R = 0,9848. Les résultats du test G-17 sont comparés. Une régression linéaire est utilisée pour étudier leur comparabilité. Les coefficients de corrélation des deux tests sont respectivement y = 0,983X + 0,079 et R = 0,9864.
Vous pourriez aussi aimer :