Bona Kvalito Ĉinia HCV Rapida Teststrio/Kasedo Entreprena Normo
Kun nia gvida teknologio samtempe kun nia spirito de novigado, reciproka kunlaboro, avantaĝoj kaj disvolviĝo, ni konstruos prosperan estontecon kune kun via estimata entrepreno por Bona Kvalito Ĉinia HCV Rapida Teststrio/Kasedo Entreprena Normo. Estante juna kreskanta organizo, ni eble ne estas la plej bonaj, sed ni klopodas nian plej bonan por esti via tre bona partnero.
Kun nia gvida teknologio samtempe kun nia spirito de novigado, reciproka kunlaboro, avantaĝoj kaj disvolviĝo, ni konstruos prosperan estontecon kune kun via estimata entrepreno porKontraŭ-HCV-N-oj, Ĉinia Hepatito C VirusoNi ĉiam insistas pri la administrada principo "Kvalito estas unua, Teknologio estas bazo, Honesteco kaj Novigado". Ni sukcesis kontinue disvolvi novajn produktojn kaj solvojn al pli alta nivelo por kontentigi la diversajn bezonojn de klientoj.
Nur por diagnoza uzo en vitro
Bonvolu atente legi ĉi tiun pakfolieton antaŭ uzo kaj strikte sekvi la instrukciojn. Fidindeco de la analizrezultoj ne povas esti garantiita se ekzistas iuj devioj de la instrukcioj en ĉi tiu pakfolieto.
INTENCITA UZO
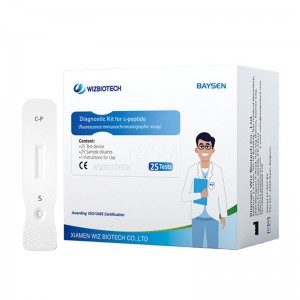
Diagnoza Ilaro por Hepatito C Virusa Antikorpo (Fluoreska Imunokromatografia Analizo) estas fluoreska imunokromatografia analizo por la kvanta detekto de HCV-antikorpo en homa serumo aŭ plasmo, kiu estas grava helpa diagnoza valoro por infekto kun hepatito C. Ĉiu pozitiva specimeno devas esti konfirmita per aliaj metodologioj. Ĉi tiu testo estas destinita nur por uzo de sanprofesiuloj.
1. Metu flanken ĉiujn reakciilojn kaj specimenojn ĝis ĉambra temperaturo.
2. Malfermu la Porteblan Imunanalizilon (WIZ-A101), enigu la konton, pasvorton kaj ensaluton laŭ la funkciigmetodo de la instrumento, kaj eniru la detektan interfacon.
3. Skanu la identigan kodon por konfirmi la testan objekton.
4. Elprenu la testkarton el la aluminia saketo.
5. Enigu la testkarton en la kartfendon, skanu la QR-kodon kaj determinu la testan objekton.
6. Aldonu 20 μL da serumo- aŭ plasmo-specimeno al la specimen-diluilo, kaj bone miksu.
7. Aldonu 80μL da specimensolvaĵo al la specimenputo de la karto.
8. Alklaku la butonon "norma testo", post 15 minutoj, la instrumento aŭtomate detektos la testkarton, ĝi povos legi la rezultojn de la ekrano de la instrumento, kaj registri/presi la testrezultojn.
9. Legu la instrukciojn de la Portebla Imunanalizilo (WIZ-A101).
RESUMO
La hepatito C viruso (HCV) estas koverta, unu-fadena pozitive sensa RNA (9.5 kb) viruso apartenanta al la familio Flaviviridae. Ses ĉefaj genotipoj kaj serioj de subtipoj de HCV estis identigitaj. Izolita en 1989, HCV nun estas agnoskita kiel la ĉefa kaŭzo de transfuzio-rilata ne-A, ne-B hepatito. La malsano karakteriziĝas per akuta kaj kronika formoj. Pli ol 50% de la infektitaj individuoj evoluigas severan, vivminacan kronikan hepatiton kun hepatcirozo kaj hepatocelulaj karcinomoj. Ekde la enkonduko en 1990 de kontraŭ-HCV-rastrumo de sangodonacoj, la incidenco de ĉi tiu infekto ĉe transfuzricevantoj signife reduktiĝis. Klinikaj studoj montras, ke signifa kvanto da HCV-infektitaj individuoj evoluigas antikorpojn kontraŭ NS5, la ne-struktura proteino de la viruso. Por tio, la testoj inkluzivas antigenojn el la NS5-regiono de la virusgenaro aldone al NS3 (c200), NS4 (c200) kaj la Kerno (c22).
PRINCIPO DE LA PROCEDURO
La membrano de la testaparato estas kovrita per HCV-antigeno sur la testa regiono kaj kapra kontraŭ-kunikla IgG-antikorpo sur la kontrolregiono. La etikedkuseneto estas antaŭe kovrita per fluoreske markita HCV-antigeno kaj kunikla IgG. Kiam oni testas pozitivan specimenon, la HCV-antikorpo en la specimeno kombiniĝas kun fluoreske markita HCV-antigeno kaj formas imunmiksaĵon. Sub la ago de imunokromatografio, la kompleksa fluo en la direkto de sorba papero, kiam la komplekso trapasas la testan regionon, ĝi kombiniĝas kun la kovranta antigeno de HCV-antigeno, formas novan komplekson. La nivelo de HCV-antikorpo estas pozitive korelaciita kun fluoreska signalo, kaj la koncentriĝo de HCV-antikorpo en la specimeno povas esti detektita per fluoreska imunanalizo.
REAGENTOJ KAJ MATERIALOJ PROVIZITAJ
25T pakaĵkomponantoj:
.Testkarto individue en folio-saketo kun sekigilo
Specimenaj diluiloj
.Pakaĵa enigaĵo
MATERIALOJ BEZONATAJ SED NE PROVIZITAJ
Ujo por specimenkolekto, tempmezurilo
SPECIMENA KOLEKTO KAJ STOKADO
1. La testitaj specimenoj povas esti serumo, heparina antikoagula plasmo aŭ EDTA antikoagula plasmo.
2. Laŭ normaj teknikoj, kolekti specimenon. Serumo- aŭ plasmospecimeno povas esti konservita fridigite je 2-8 ℃ dum 7 tagoj kaj kriokonservado sub -15 °C dum 6 monatoj.
3. Ĉiuj specimenoj evitas frostig-degelajn ciklojn.
PROCEDURA ANALIZO
Bonvolu legi la instrumento-funkciigan manlibron kaj la pakaĵinserton antaŭ ol testi.
Ĉi tiu testrezulto estas nur por klinika referenco, ne devus servi kiel la sola bazo por klinika diagnozo kaj kuracado. La klinika administrado de la paciento devas esti ampleksa konsidero kombinita kun ĝiaj simptomoj, medicina historio, aliaj laboratorio-ekzamenoj, kurac-respondo, epidemiologio kaj aliaj informoj.
Ĉi tiu reakciilo estas uzata nur por serumaj kaj plasmaj testoj. Eble ĝi ne donos precizajn rezultojn kiam uzata por aliaj specimenoj kiel salivo kaj urino ktp.
EFIKAJ KARAKTERISTIKOJ
| Lineareco | 0,005-5 | relativa devio: -15% ĝis +15%. |
| Lineara korelacia koeficiento: (r) ≥ 0,9900 | ||
| Precizeco | La reakiro-procento devas esti inter 85% kaj 115%. | |
| Ripeteblo | KV≤15% | |
REFERENCOJ
1. Posttransfuzia hepatito. En: Moore SB, red. Transfuz-Transdonitaj Virusaj Malsanoj. Alington, VA. Am. Assoc. Sangobankoj, pp. 53-38.
2. Hansen JH, et al. HAMA-Interfero kun Murinaj Monoklonaj Antikorpaj Imunanalizoj [J]. J of Clin Immunoassay, 1993, 16:294-299.
3. Levinson SS. La Naturo de Heterofilaj Antikorpoj kaj la Rolo en Imunanaliza Interfero [J]. J de Clin Immunoassay, 1992, 15:108-114.
4. Alter HJ., Purcell RH, Holland PV, et al. (1978) Transdonebla agento en ne-A, ne-B hepatito. Lancet I: 459-463.
5. Choo QL, Weiner AJ, Overby LR, Kuo G, Houghton M. (1990) Hepatito C Viruso: la ĉefa kaŭza agento de virusa ne-A, ne-B hepatito. Br Med Bull 46: 423-441.
6. Engvall E, Perlmann P. (1971) Enzim-ligita imunosorba analizo (ELISA): kvalita analizo de IgG. Immunochemistry 8:871-874.
ATENDATAJ VALOROJ
HCV-Ab<0.02
Estas rekomendinde, ke ĉiu laboratorio establu sian propran normalan intervalon reprezentantan sian pacientaron.
TESTREZULTOJ KAJ INTERPRETADO
- La supraj datumoj estas la rezulto de la testo per HCV-Ab-reakciaĵo, kaj oni sugestas, ke ĉiu laboratorio establu gamon de HCV-Ab-detektaj valoroj taŭgaj por la loĝantaro en ĉi tiu regiono. La supraj rezultoj estas nur por referenco.
- La rezultoj de ĉi tiu metodo aplikeblas nur al la referencaj intervaloj establitaj en ĉi tiu metodo, kaj ne ekzistas rekta komparebleco kun aliaj metodoj.
- Aliaj faktoroj ankaŭ povas kaŭzi erarojn en detektorezultoj, inkluzive de teknikaj kialoj, funkciaj eraroj kaj aliaj provaĵaj faktoroj.
STOKADO KAJ STABILECO
- La ilaro havas daŭron de konservo de 18 monatoj ekde la fabrikada dato. Konservu neuzitajn ilarojn je 2-30 °C. NE FROSTU. Ne uzu post la eksvalidiĝdato.
- Ne malfermu la sigelitan saketon ĝis vi pretas fari teston, kaj la unu-uzan teston oni sugestas uzi sub la bezonata medio (temperaturo 2-35℃, humideco 40-90%) ene de 60 minutoj kiel eble plej rapide.
- Provaĵdiluilo estas uzata tuj post malfermo.
AVERTOJ KAJ ANTAŬZORGOJ
La ilaro estu sigelita kaj protektita kontraŭ humideco.
Ĉiuj pozitivaj specimenoj devas esti validigitaj per aliaj metodologioj.
.Ĉiuj specimenoj estu traktataj kiel eblaj poluantoj.
.NE uzu eksvalidiĝintan reakciaĵon.
.NE interŝanĝu reakciilojn inter ilaroj kun malsama lotnumero..
.NE reuzu testkartojn kaj iujn ajn forĵeteblajn akcesoraĵojn.
.Misfunkciado, troa aŭ malgranda specimeno povas konduki al rezultaj devioj.
LIMITAĴO
.Kiel ĉe iu ajn analizo uzanta musajn antikorpojn, ekzistas la ebleco de interfero fare de homaj kontraŭmusaj antikorpoj (HAMA) en la specimeno. Specimenoj de pacientoj, kiuj ricevis preparojn de monoklonaj antikorpoj por diagnozo aŭ terapio, povas enhavi HAMA. Tiaj specimenoj povas kaŭzi falspozitivajn aŭ falsnegativajn rezultojn.
Klarigo de uzitaj simboloj:
 | En Vitro Diagnoza Medicina Aparato |
 | Fabrikisto |
 | Konservu je 2-30℃ |
 | Finvalida dato |
 | Ne Reuzu |
 | ATENTU |
 | Konsultu Instrukciojn Por Uzo |